今回は勉強モードとして最後のブログになります。内容は「制御性T細胞」に関するものです。
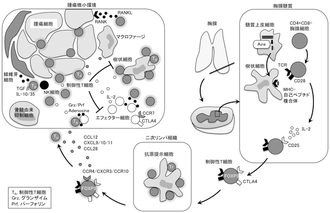
国立がん研究センターのホームページにも「がんと制御性T細胞」と題するページがあり、その中で『がん細胞に対する免疫応答のなかでも注目を集めているのが、制御性T細胞と呼ばれる免疫抑制細胞です』との記述があります。また、下記はそのページに出ている「がんにおけるT細胞」のイラストです。

出版:講談社(ブルーバックス)
発行:初版2016年1月20日
大項目は次の通りです。
プロローグ
第1章 樹状細胞の物語
第2章 制御性T細胞の物語
第3章 成人性T細胞白血病との戦いの物語
第4章 免疫チェックポイントの物語
第5章 インターロイキン6の物語
エピローグ
ブログでは「プロローグ」の全文、「第2章 制御性T細胞の物語」および「エピローグ」のそれぞれ一部をご紹介させて頂きます。
なお、「第2章 制御性T細胞の物語」の中の内容は以下になります。青字になっているのがブログで取り上げた項目です。
第2章 制御性T細胞の物語
●「撃ち方やめ」を周知徹底
●大学院をあっけなく中退
●愛知県がんセンターのユニークな報告
●一世を風靡した抑制性T細胞
●坂口の前に現れた抑制性T細胞
●「細胞はCD8ネガティブ」
●「これだけは譲れない」
●学会から急に消えた抑制性T細胞
●運に恵まれ奨学金を手に
●米国でマーカーにメド
●免疫抑制剤で自己免疫疾患が起きる?
●IL2抑制で制御T細胞が減少
●シェバックの宗旨替えで追い風
●筑波で医薬品企業に売り込み
●医療応用の青写真
●「CD25」論文執筆を決意
●英『ネイチャー』から門前払い
●シェバックが直ちに追認
●『セル』に制御性T細胞登場
●抗原提示の分子メカニズム
●イス取りゲームで免疫を抑制
●制御性T細胞が存在する証拠
●関節リウマチを発症するSKGマウス
●SKGマウスの効用
●ファントム坂口
●マスター遺伝子の発見
●Foxp3遺伝子で制御性T細胞に変身
●生きた動物でも証明
●医療応用を目指して
プロローグ
一度かかった病気には、次はかからない。二度目の「疫」病からは「免」れる。「免疫」という言葉には、そんな意味が込められている。
そうした免疫の働きを担う主役の一つを人類が突きとめたのは、いまから百年以上も前のことだった。日本の北里柴三郎が、破傷風菌の毒素を中和する抗毒素 ―現代の私たちが「抗体」と呼ぶ免疫分子― を、留学先のドイツで発見したのである。
北里は残念ながらノーベル賞を逃したが、彼の“弟子”は長い時を経て師の無念を晴らした。北里研究所で研究に励み、微生物から感染症の特効薬を探り当てた大村智(北里大学特別栄誉教授)が、2015年にノーベル生理学・医学賞を受賞したのだ。
抗体のたぐいまれな働きは、西アフリカでエボラ出血熱が猛威をふるったときにも世界を刮目させた。運よく生き残った人の血液から抗体を含む血清が取り出され、患者の治療に使われたのだ。北里が考案した血清療法である。
北里から始まる現代免疫学の歩みは、私たちに「抗体医薬」という良薬ももたらした。異物を捕まえる抗体の性質を利用して、関節リウマチなどの自己免疫疾患やがんを治療する医薬だ。
抗体だけではない。人の体の中ではさまざまな免疫細胞が、外部から侵入した病原体や、頻繁に発生するがん細胞と戦いつづけている。外の敵にも、内の敵に対しても、免疫はさまざまな手段を駆使して、人類という種を守ってきてくれたのだ。
免疫の舞台で主役級の活躍をするものの一つが「樹状細胞」と呼ばれる免疫細胞だ。体の中をパトロールして、侵入した病原体を長い腕で捕まえると、「こいつが敵だ」といって仲間の免疫細胞に“見せ”にいく細胞である。
樹状細胞のこうした営みは「抗原提示」と呼ばれる。「抗原」とは病原体が持つ印のこと。何はともあれ、わが身を襲撃してきた犯人の顔がわからなければ、免疫はことを起こせない。その点で樹状細胞は、免疫に欠くべからざる存在なのだ。
抗原提示の営みは、何によって、どのように行われているのか。こうした根源的な疑問と謎に魅了され、一生をかけて樹状細胞を隅々まで調べ尽くしたのは、京都大学の稲葉カヨとカナダのラルフ・スタインマンだった。
樹状細胞に勝るとも劣らず、生命科学の教科書を塗り替える働きを持つ免疫細胞も、日本人によって見つかった。敵を攻撃しようとする免疫の営みを抑制する「制御性T細胞」だ。大阪大学の坂口志文が、日米を転々としながら、約三十年もの歳月をかけて突きとめたユニークな細胞である。
せっかく病原体と戦っている免疫細胞の足を、わざわざ引っ張らくともよいではないかと思われるかもしれない。だが、その行動には合理的な理由がある。
びっくりされるかもしれないが、私たちの体の中には、わが身の臓器や組織を敵とみなして攻撃する恐ろしい自己反応性の免疫細胞が少なからずいる。そして、攻撃好きなそれらの免疫細胞は、骨や関節を破壊する関節リウマチなど、さまざまな自己免疫疾患を引き起こすこともわかってきた。
そこで、こうした“身内の凶悪犯”を封じるべく、免疫があらかじめ備え持っているのが制御性T細胞。自己反応性の免疫細胞が悪さをしはじめると、この細胞が現れ「攻撃中止」を命令するのだ。
ところが、話はこれだけでは終わらない。実は制御性T細胞は、あってはならない悪事の犯人でもあるからだ。専門家の間では、この細胞はがん細胞の“盾”となって、がん細胞を攻撃しようとする免疫細胞の邪魔をすることが知られている。
こんな不可解で奇妙な制御性T細胞のふるまいの謎は、現在では分子レベルで解明されている。制御性T細胞は「免疫チェックポイント分子」といって、自動車にブレーキをかけるように免疫細胞の攻撃を制止する特殊な分子を備え持っていたのだ。
免疫チェックポイント分子はいわばブレーキ・ボタン。制御性T細胞とは、生まれたときからずっと、このボタンを持つよう運命づけられた免疫細胞なのだ。
この特異な分子は、他の免疫細胞の表面に一時的に現れることもある。たとえばキラーT細胞といって免疫細胞の中で殺し屋の異名を持つ細胞が、がん細胞と戦いはじめたとしよう。このとき、敵を退治したあとも攻撃を続け、正常な細胞を傷つけるなどの「やりすぎ」が起きては困る。そこで免疫は、頃合いみて「撃ち方やめ」のシグナルを出す免疫チェックポイント分子を、臨機応変にキラーT細胞の表面に現れるようにした。
ところが、がんの悪知恵もすごい。がん細胞は、キラーT細胞の攻撃を受けると自分の体の表面にチェックポイント分子と結合する分子を出現させ、キラーT細胞の攻撃をストップさせてしまうのだ。
狡猾ながんの戦術に気づいた免疫研究者や医者の関心は、免疫チェックポイント分子へと向かった。がんがそこまでやるのなら、我々はブレーキを悪用されないようにボタンをブロックする抗体医薬をつくろう。そうすれば、免疫細胞はノンストップでがんと戦ってくれる ―という作戦である。
いま、最も注目を集めている免疫チェックポイント分子は、日本の本庶佑が京大の教授時代に偶然、発見したPD-1という分子だ。そして、PD-1に注目してがん治療のための抗体医薬を開発したのもまた、日本の製薬企業だった。
がんとの戦いに比べると派手さはないかもしれないが、現代免疫学は、原因が不明で治療が難しかった難病にも堅実に迫りつつある。免疫細胞の過度な攻撃によって起こる自己免疫疾患性の難病も、次第に抗体医薬によって症状を改善できるようになってきたのだ。
これから語るのは、日本の研究者たちの不断の努力と活躍を縦糸に、最新の成果を横糸に織り込んで紡ぎ出した、現代免疫学の物語。読者ははるかな過去から私たちの生命と健康を守りつづけてきた免疫がいま、がんや難病の制圧に挑み、かつてない成果をあげはじめたことに息を呑まれるだろう。
第2章 制御性T細胞の物語
●「撃ち方やめ」を周知徹底
これから語るのは、大阪大学教授の坂口志文が発見した「制御性T細胞」の物語だ。独自の研究を積み重ね、免疫学の常識を覆した坂口の研究人生を縦糸に、制御性T細胞の不思議な営みを横糸にして、物語を紡いでいく。
最初に、制御性T細胞のおおよその働きをお伝えしておこう。坂口に言わせると、敵の襲撃から生命体を守る免疫のしくみは、西部劇の保安官そっくりだ。平和な町にやってきた“ならず者”の病原菌やウィルスを、保安官がきっちりやっつけてくれるからだ。
だが、私たちの体の中の保安官はときに、かなり粗雑な行動をとることもあるらしい。乱暴者を見つけて攻撃を始めたのはよいのだが、頭に血が上って冷静さを失い、過剰な発砲をやめられなくなってしまうのだ。
とばっちりを受けるのは近隣にいる町の住民で、保安官が乱暴者めがけて撃ったはずの銃弾を浴びてしまう。さらに恐ろしいことに、住民をならず者と見誤って痛めつけてしまうケースも少なからず起こっているらしい。
免疫細胞は誕生した直後に、胸腺という特殊な組織で身内の「顔」をしっかり記憶し、仲間を決して攻撃しないように教育されている、とかつての免疫学は教えてきた。

画像出展:「免疫が挑むがんと難病」
下記をクリック頂くと、NCBI(National Center for Biotechnology Information)に掲載されている論文のページが表示されます。
だが、いささか楽観的すぎたようだ。最近の研究では、胸腺にも手抜かりや不手際が少なからずあり、教育不行き届きの免疫細胞を送り出していることがわかってきた。私たちの体にはわが身を敵とみなす恐ろしい自己反応性の免疫細胞がたくさんうろついていて、正常な臓器や組織を攻撃していたのだ。
おっかない保安官ならぬ免疫細胞たちがそうやって実際に引き起こす病気が、自己免疫疾患なのである。
骨が溶け、最後に関節まで破壊されてしまう関節リウマチ、膵臓のインスリン生産細胞が破壊されてしまう1型糖尿病、脳や脊髄の神経細胞を覆う膜が攻撃されて多発性の硬い病巣組織ができる多発性硬化症など枚挙にいとまがない。
しかし、免疫は自らの不完全さを意識していたのか、自らのしくみの中に、不思議な細胞を内在させていた。免疫の働きが過剰になったり、自己反応性の免疫細胞が悪さを始めたりしたときに、やりすぎを抑制して「撃ち方やめ」を周知徹底させる役割を担う細胞だ。それが、坂口が発見した制御性T細胞である。
もし制御性T細胞がなかったら、免疫細胞はブレーキをかけられない車のように暴走し、いまよりもはるかに多くの人が自己免疫疾患で苦しむことになっただろう。制御性T細胞の功績は実に大きい。
しかし、私たちの体はこのような安全弁のような細胞を持ったことで、その代償も支払わねばならなくなった。あろうことか、この細胞は体にできたがん細胞の“盾”となって、がん細胞を攻撃しようとする免疫細胞の邪魔をしてしまうのだ。まるでその様子は、悪者の用心棒。生き物の体の不思議さと理不尽さはここに極まれり、だ。
だからいま、研究者や製薬会社の関心は、制御性T細胞の悪さをいかに封じるかに向かう。前章で紹介したスタインマン(ラルフ・マーヴィン・スタインマン。カナダの免疫学者、細胞生物学者。2011年にノーベル生理学・医学賞を受賞)の闘病を語った際に紹介した抗体医薬ヤーボイも、実はそうした働きを備えた新しいがん治療なのだ。

ノーベル医学生理学賞を受賞された本庶佑先生が発見したのは免疫チェックポイント分子のPD-1。そして抗PD-1抗体の製品名が「オプジーボ」。
一方、製品名「ヤーボイ」は免疫チェックポイント分子、CTLA4をターゲットとした製品。
いずれも「免疫チェックポイント阻害薬」であり、仲間ということになります。
画像出展:「AnswersNews」
坂口は京都大学の医学部を卒業した直後に制御性T細胞の研究にのめりこみ、日米を転々としながら四半世紀もの歳月をかけて、その存在を実証した不屈の研究者だ。読者はこれから始まる物語を読んで、坂口の歩んだ道のりの険しさと、制御性T細胞によって描き直された免疫の世界の不思議な営みに、きっと驚嘆されることだろう。
●一世を風靡した抑制性T細胞
ここで、時計の針を十年ほど逆に回してみよう。なぜかというと、坂口の人生に重大な影響を及ぼすことになる免疫細胞が、その時期に発表されているからだ。それは制御性T細胞に先駆けて、免疫の営みを抑制する細胞として一世を風靡した「抑制性T細胞」(サプレッサーT細胞)である。
抑制性T細胞というアイデアを最初に唱えた研究者は、日本の多田富雄や米エール大学のリチャード・ガーションたちだった。
多田が抑制性T細胞を唱えるきっかけとなったのは、1968年に千葉大学で始めたある実験だった。
多田はこれに先立つ米国留学で、アレルギーを引き起こすIgE抗体を発見し世界に名をとどろかせた石坂公成に師事していた。そんな彼は日本に戻るや、IgE抗体と二つの免疫細胞(T細胞とB細胞)の関わりに焦点を当てた研究を開始した。
「このような研究はまだ誰もやっていない。先頭を走るのは自分だ」。多田は自信満々だった。
だが、IgE抗体の量を測定してみると、IgE抗体は一時的に増加するものの、すぐに減ってしまったのだ。
さらに多田たちをとまどわせる現象も起きた。IgE抗体の量を減らすためにX線を照射したり胸腺を摘出したりすると、逆にIgE抗体の数値が異常に高くなるというデータが現れたのだ。いったい何が起きているのか、多田は頭を抱えてしまった。
多田がのちに千葉大学で行った講演によると、そのアイデアは彼が朝風呂に入っているときにひらめいたのだという。「ひょっとしたら僕たちはX線照射や胸腺摘出によって、免疫の働きを抑制する細胞を減らしていたのではないか」と。
多田は自宅から研究室に駆けつけると、ただちに実験を開始した。胸腺を摘出されてIgE抗体の量が異常に増えたネズミに、正常なネズミの胸腺を移し入れる実験である。
結果は劇的だった。IgE抗体の数値は思ったとおり、大幅に下がってくれた。胸腺の移植によって出現した未知の免疫細胞が、B細胞が抗体をつくり出す営みにブレーキをかけたのだ、多田は確信した。
1971年に米国のワシントンで開催された第一回国際免疫学会において、多田は意気揚々と「免疫の働きを抑制する抑制性T細胞を発見した」と発表した。抑制性T細胞という新たな免疫細胞の出現に聴衆は驚き、1970年代は「サプレッサー・エイジ」と呼ばれるほど、研究者の間で抑制性T細胞の研究は大流行するにいたった。
実は、抑制性T細胞という言葉もサプレッサーT細胞という言葉も、現在では死後に近い。だが、「免疫の働きを抑制する細胞」という基本的な概念の創始者の一人はまぎれもなく多田だった。いまから40年以上も前に新しい概念を提唱した彼の卓越した先見性に敬意を表したい。
●坂口の前に現れた抑制性T細胞
国際免疫学会で多田が喝采を浴びていた頃、坂口は医学部に入学したばかりの学生だった。この時期はまだ免疫への関心はあまりなく、抑制性T細胞という概念さえ知らない青二才だった。
その坂口が免疫に好奇心を持ったのは、IgE抗体を発見した石坂公成が京大の教授に就任するといった噂がキャンパスに流れた頃だっただろうか。折しも坂口は、妊婦の免疫が胎児を攻撃しない免疫寛容や、逆に免疫が自分の臓器や組織を攻撃する自己免疫疾患の話題を講義で聞き、次第に好奇心を持つようになっていた。
この時期、免疫学会のシンポジウムに顔を出してみると、流行のサプレッサーT細胞の話題で参加者はとても盛り上がっていたという。
1980年、坂口は愛知県がんセンターを去り、京大に戻ってきた。医学部の免疫研究施設に体をいったん落ち着け、ここで博士号を取得するための論文を執筆しようとしたのだった。
論文のテーマはもう決めていた。がんセンターでの研究成果をそのまま書こうというのだ。だが、これは坂口にとってただならぬ選択だった。なぜなら彼が見つけた制御性T細胞は、多田の唱える抑制性T細胞とは似て非なるものだったからだ。
このとき、すでに多田の抑制性T細胞は世界でメジャーな存在となっていた。坂口はこれから書く論文の中で、超大物の細胞と対峙しなければならなかった。
詳しく事情を説明しよう。細胞の表面には、その細胞が持つ特徴を表す細胞表面分子(CD:CDの「C」は「群れ、集団」を表すclusterの頭文字。「D」は「分化、差異、派生」といった意味を持つdifferentiationの頭文字)が顔を出している。これをマーカーとして使えば、免疫細胞も簡単に分類することができる。
坂口が愛知県がんセンターにいた時期は、T細胞のマーカーがある程度、判明しつつあった頃だった。たとえば免疫系の司令塔といわれるヘルパーT細胞のマーカーは「CD4」であることがわかってきた。また、ウィルスに感染した細胞やがん細胞を攻撃するキラーT細胞は「CD8」を持っているとの報告も現れていただろうか。
マーカーに注目した呼び方をするなら、ヘルパーT細胞は「CD4・T細胞」であり、キラーT細胞は「CD8・T細胞」である、というわけだ。
ならば、坂口が突きとめた新種の免疫細胞(つまり制御性T細胞)の正体は何なのだろうか。私たちはつい先ほど、この新しい細胞は「CD4・T細胞」だと語ったばかりだ。坂口はこの細胞の表面にCD4を見つけていたのだ。ならば制御性T細胞は、同じく表面にCD4を持つヘルパーT細胞と同種の細胞なのだろうか。
いや違う。制御性T細胞の表面には確かにCD4はあるが、実はそれ以外に「CD25」という分子も存在していたのだ。つまり制御性T細胞はヘルパーT細胞とは異なる細胞であり、「CD4・CD25・T細胞」と呼ぶべき存在だったのだ。ちなみに、CD25は坂口が1995年に、制御性T細胞と他のT細胞を識別するための重要なマーカーとして発表する細胞表面分子である。
●医療応用の青写真
制御性T細胞はどのような医療応用ができるのだろうか。当時、坂口の脳裡に浮かんだいくつかのアイデアを語ってみよう。
まず、制御性T細胞による過剰な免疫反応の抑制。私たちの体は免疫細胞が病原体を攻撃してくれるおかげで感染症から守られている。しかし免疫の営みが強いせいで起きる病気もある。花粉症などのアレルギーや関節リウマチのような自己免疫疾患だ。
だが制御性T細胞を活用して免疫の攻撃を抑制すれば、アレルギーも自己免疫疾患も治療できる可能性がある。体内の制御性T細胞を取り出して、体外で増やしてから体に戻すといった方法が確立すれば、治療は現実のものとなるだろう。
臓器移植への応用も視野に入る。臓器提供者(ドナー)の臓器を患者に移植すると、多かれ少なかれ拒絶反応が起こる。患者の体の免疫細胞が、移植された臓器を異物とみなし攻撃を始めるせいだ。
しかしこの反応も、制御性T細胞によって抑制することができるかもしれない。うまくいけば、近未来には免疫抑制剤を使わずに臓器移植ができるようになる可能性がある。
また、骨髄移植では、通常の拒絶反応とは異なり、移植された骨髄から生まれた免疫細胞が患者の体を異物とみなして攻撃する移植片対宿主病が起きる。だが、これも制御性T細胞によって抑制できるはずだ。
制御性T細胞の働きを弱めることでも、さまざまな応用が見えてくる。たとえば感染力や攻撃力がとても強い病原体がもたらす感染症の治療では、一時的に制御性T細胞の働きを弱めて、病原体と戦う免疫細胞の攻撃力を強めれば効果的かもしれない。
敵は体の外からやってくる病原体だけではない。体の内にはがん細胞という凶悪な敵がいる。しかも狡猾ながん細胞は、制御性T細胞をうまく手なずけて自分の味方にしてしまい、免疫細胞の攻撃から免れる術も体得している。
ならば、がんとの戦いで有効な方策は、がん細胞の味方に回った制御性T細胞の動きを阻害することだ。こうした働きを備えた新薬が、スタインマンが使ったヤーボイだった。
●「CD25」論文執筆を決意
坂口がようやく雇用期限のない安定した地位を手に入れたのは、1995年のことだった。彼は東京都老人総合研究所で免疫病理部門長というポストを獲得した。彼が生まれて初めてボーナスをもらったのもこの研究所だった。坂口はここで、いよいよ長年の研究の集大成ともいうべき研究論文を書くことを決意する。
論文を発表してから16年後の2011年4月号で『米国免疫学会誌』が「免疫学で一時代を画した論文(Pillars Articles in Immunology)」と最大級の評価をした論文である。
その頃までに坂口が突きとめていた事実をひとまず、まとめておこう。
まず、制御性T細胞はCD4とCD25という二つの細胞表面分子を備えた免疫細胞だった。免疫の司令塔とされるヘルパーT細胞も、CD4を持っているし、刺激を受ければCD25が発現することもある。しかし、制御性T細胞は生まれつきCD25を備えている。これが二つの細胞の決定的な違いだ。
また、しばらく前に語ったようにCD25の正体は、IL2受容体のα鎖であることも判明していた。制御性T細胞が胸腺で常に生まれつづけていることもわかった。
CD25のマーカーとしての能力は卓越していた。坂口はこれまでの研究で制御性T細胞の選別に役立ちそうな分子をいくつか見つけていたが、CD25はそれらの候補を凌駕していた。
●イス取りゲームで免疫を抑制
さて、そこで制御性T細胞と免疫チェックポイント分子のCTLA-4だ。この分子はいったいどうやって免疫の営みを抑制するというのだろうか。
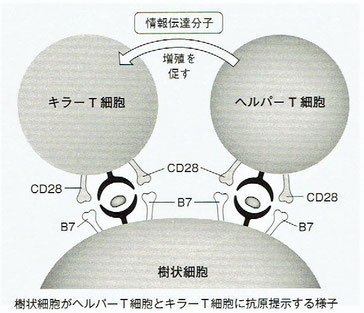
イラストをご覧いただきたい。これは体内で病原体を発見した樹状細胞が、その断片を掲げて免疫の司令塔ヘルパーT細胞のもとに抗原提示をしようとやってきた場面である。
樹状細胞の右上にのっているのがヘルパーT細胞だ。先ほど語ったように、ヘルパーT細胞の表面からは副刺激分子のCD28が出ていて、樹状細胞の表面からは補助副刺激分子B7が出ている。抗原提示のプロセスが終わり、CD28とB7が結びついて補助シグナルが流れると、いよいよ戦闘開始だ。
やや専門の度が強いかもしれないが、実はこのとき、キラーT細胞もヘルパーT細胞と同様に樹状細胞とつながっていて、抗原提示を受けている。すると、ヘルパーT細胞は近くにいるキラーT細胞に向かって情報伝達分子を放出して増殖を促す。こうしてキラーT細胞は大部隊に膨れあがり、がんとの戦いに出動することとなる。
ところが、ここに制御性T細胞が現れると、ヘルパーT細胞やキラーT細胞にとって面倒な事態が生じる。上のイラストのように樹状細胞の上に制御性T細胞がのしかかって“合体”して、抗原提示の妨害をするからだ。
このとき制御性T細胞の“武器”が、CTLA-4分子。制御性T細胞はこの分子を使って、樹状細胞の表面に出ているB7分子と結びついてしまうのだ。これは、本来であればヘルパーT細胞やキラーT細胞が落ち着くべき場所を、制御性T細胞が“横取り”したことにほかならない。
制御性T細胞の数が少なければ、ヘルパーT細胞などの受ける影響は少なくてすむ。しかし、制御性T細胞が大挙してやってきたときは具合が悪い。しかも、樹状細胞との相性は、制御性T細胞のほうがヘルパーT細胞よりも優っている。そもそも制御性T細胞の表面にはCTLA-4分子が多く出ているうえに、接着分子といって、文字どおり樹状細胞と接着する分子も発現しているからだ。
こうして、制御性T細胞が樹状細胞の表面を覆いつくしたとしよう。そうなるともはや、ヘルパーT細胞などには樹状細胞と物理的に接触する余地がなくなってしまう。
つまり、制御性T細胞と他のT細胞の関係は、限られた席を争ってイス取りゲームをしているライバルどうし。制御性T細胞の群れが大きいと、その分、ヘルパーT細胞などのT細胞は樹状細胞と合体できなくなって、抗原提示が阻害され、免疫の営みが低下してしまうのだ。
制御性T細胞はイス取りゲームのイスをただ奪うだけでなく、イスの数そのものを減らすことで抗原提示を阻害していることもわかっている。
このプロセスでも暗躍するのはCTLA-4分子。この分子を介して制御性T細胞が樹状細胞とつながると、樹状細胞は表面に補助刺激分子のB7を発現しなくなってしまう。そうなるとヘルパーT細胞には補助シグナルが入らず、抗原提示を受けても戦闘開始の命令を出せなくなってしまうのだ。
●制御性T細胞が存在する証拠
がんになった人の体では、キラーT細胞ががん細胞をやっつけようとしても、制御性T細胞に邪魔されてしまう。免疫細胞の過度の攻撃を防ぐのが自分の任務と心得た制御性T細胞が、がん細胞の“盾”のようにキラーT細胞の営みを抑制するからだ。
ヤーボイとは、そうした制御性T細胞の悪事を封じるための抗体医薬。制御性T細胞の表面にある免疫チェックポイント分子のCTLA-4分子をブロックするモノクローナル抗体をつくり、これをがん治療用の医薬としたものだ。
だが、ヤーボイは強い副作用を伴う医薬でもある。ヤーボイの働きによって制御性T細胞の営みが封じられると、免疫細胞が激しく腸管組織を攻撃する結果、お腹の調子が乱れてただならぬ下痢や腹痛が起きる。
実際、(ヤーボイを服用していた)スタインマンは激しい下痢に襲われ、あまりの副作用の強さに治療の継続を断念してしまったという。制御性T細胞が確かに存在することを示す生々しい証拠といえるだろう。
スタインマンがヤーボイの投与を受けたのは、闘病生活の後期の頃だったといわれる。体がもっと元気な頃であれば副作用を我慢することができ、がんとの戦いをもっと有利に展開できたかもしれない。
制御性T細胞が備えるCTLA-4分子は最近、がんの免疫療法への応用で急速に注目を集めている。免疫チェックポイント分子は他に仲間もいる。その一例はPD-1分子で、スタインマンは一時、この分子をブロックする抗体医薬の利用も検討した、と伝えらえる。PD-1は1990年代に京大の本庶佑らが発見した分子だ。がんの免疫療法とは切っても切れない制御性T細胞や免疫チェックポイント分子については、のちにあらためて、たっぷり語ることにしよう。
エピローグ
いつの頃か、生き物の中には体内に細菌を取り込み、共生関係を築くものが現れた。その関係は生命の進化が進んでも延々と受け継がれ、人という種もまた、天文学的な種類と数の細菌を腸内に棲まわせるようになった。そして他の組織や臓器では細菌を攻撃する免疫も、腸の中ではおとなしく襲撃を慎む大人の知恵を身につけた。
胎児への攻撃自制も、細菌との共生も、専門家が「免疫寛容」と呼ぶ不思議な営みである。
なぜ、免疫は自らにブレーキをかけるのか。この問いに対する概念的な「解」は比較的、早期に現れた。1970年代に提唱された抑制性T細胞である。免疫の攻撃を抑制する特殊な細胞を免疫の一員に加えれば、免疫寛容の現象はきちんと説明がつけられたのだ。
しかし、概念と実体にはことのほか距離があった。抑制性T細胞の探索は難航し、ついには実在の証拠とされたデータが幻とわかり、研究者の関心は急速に薄れていった。「免疫寛容の時代」の始まりである。
現代免疫学がようやく深い轍を乗り越え、確かな実体を捉えることに成功したのは少なからぬ時間が流れたあとのこと。かつての有力候補とは似て非なる制御性T細胞と、制御性T細胞などの表面に現れる免疫チェックポイント分子の存在とその働きが、相次ぎ確認されたのだ。
そして、その営みに注目した抗体医薬が医療現場で使われるに及ぶと、医師や研究者は、一度は否定された「免疫にブレーキをかける」細胞や分子が実在することを文句なしに信じざるをえなくなった。
~中略~
これほどまでに存在感を高めた制御性T細胞とチェックポイント分子を前に、私たちはどのような心構えをしたらいいのだろう。一案は私たちがいま、免疫と病気をめぐる基本的なものの見方(パラダイム)が遷り変わるまっただ中にいる、と自覚することかもしれない。
免疫とはかつて、外部からやってくる病原体を攻撃し排除する防衛システムと考えられた。その防衛力を削ぎ落すブレーキの営みは、かつてなら免疫の対極に位置するものと捉えられた。
しかし、その認識のしかたはどうやら間違っていたらしい。免疫は、病原体やがんなどの敵と向き合い対峙する能力の内に、攻撃をほどほどに収めるしくみを重要な要素として含んでいたのだ。
免疫の攻撃力が強ければ、力をもてあました攻撃系の免疫細胞は身内の臓器や組織を攻撃し、深刻な自己免疫疾患を起こす。逆に攻撃力が弱くなれば、人は感染症やがんにかかりやすくなる。
私たちはこのように、免疫の両輪といえるアクセル(攻撃)とブレーキ(抑制)のバランスの中で、ある時は健康に生き、ある時は病気になったり死んだりしているのだ。
大切なのはアクセルとブレーキの平衡。両者のバランスがほどよくとれるなら私たちは、がんにかかることもなく、自己免疫疾患に悩まされることもなく天寿を全うできるだろう。
バランスが崩れてがんや自己免疫疾患になっても、私たちは徒手空拳でこれらの病気と対峙するわけではない。ブレーキを解除する新しい抗体医薬の登場によって、かつて効用が軽視されがちだったがんの免疫療法は、外科手術、放射線治療、抗がん剤と肩を並べるほどの治療成績をおさめつつあるからだ。
しばしば原因不明の難病扱いをされてきた自己免疫疾患のいくつかは、治療法がわかってきた。視神経脊髄炎や強皮症、大動脈炎症候群などの病気では、背後にインターロイキン6(IL6)という炎症性の情報伝達分子が暗躍していることが判明した。その結果、関節リウマチの治療に使う抗体医薬(アクテムラ)がこれらの病気の治療でも良好な成果を収めはじめたのだ。
バランスを欠いたアクセルとブレーキの関係を修復するための手がかりも見えてきた。私たちがお腹の中に棲まわせている腸内細菌は、ただ免疫細胞から攻撃を見合わせてもらっているだけの軟弱な存在ではなく、免疫にさまざまな刺激を与え影響を及ぼす重要な存在だった。
たとえばある種の腸内細菌がつくる酪酸は、免疫系に作用して、ブレーキ役の制御性T細胞を増やすことがわかっている。また、特定の細菌は自己免疫疾患を引き起こすヘルパーT細胞を誘導することも明らかとなった。
つまり腸内細菌は、時と場合によって免疫力の攻撃力を高めたり、逆に抑制力を強めたりしているのだ。
腸内細菌の研究が緒に就いたばかりだといって、あなどってはいけない。免疫学の畑ではないが、現代の研究者は腸内細菌の移植によって、太ったネズミと太らないネズミをつくり出しさえしている。
~以下省略~