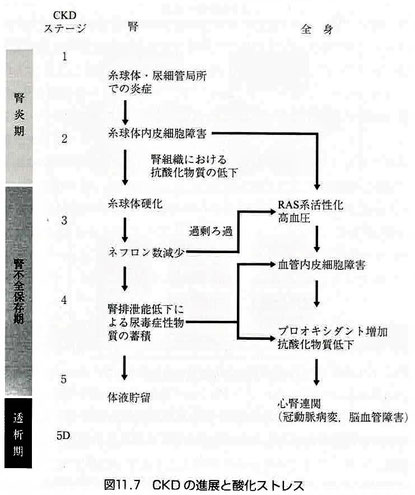
血管内皮細胞に興味をもった理由は下記の図です。
この図はブログ「腎臓疾患における活性酸素」でご紹介した『抗酸化の科学』という本の中にあったものですが、ブログ「腎臓のはなし1」でもご紹介しているため、3度目の登場となります。
CKDとは“慢性腎臓病”のことです。初期のステージ1に書かれているのは、“糸球体・尿細管局所での炎症”です。そして、ステージ2は“糸球体内皮細胞障害”となっています。
一方、下記は初登場ですが、『病気がみえる vol.8 腎臓・泌尿器』から拝借したものです。このチャートを見る限り中段左側の“内皮細胞障害”は“糸球体高血圧”に伴って発生するものとされています。
なお、この図(腎障害の進行)を載せた理由は、右上上段の●と下部●に書かれている内容が気になったためです。
●『ある程度の腎機能低下に至った後、腎障害の慢性的な進行は、原因疾患にかかわらず共通の機序で不可逆性に進むと考えられており、この機序をfinal common pathwayとよぶ。』
⇒「ある程度の腎機能低下」の“ある程度”が不明確だが、この範囲であれば不可逆性ではなく、改善が期待できるということか?
●『final common pathwayの他に、尿細管周囲毛細血管の喪失などにより尿細管間質が慢性の低酸素状態に陥るために腎障害が進行する(慢性低酸素仮説)とも考えられている。』
⇒糸球体ではなく、尿細管周囲毛細血管の問題でもクレアチニン値やeGFR値は悪化するのか?また、この尿細管周囲毛細血管の問題も糸球体同様、不可逆的と考えられているのか?

画像出展:「病気がみえる vol8 腎臓・泌尿器」
右上の[腎血管の走行]を見ると、糸球体は“第1の毛細血管”であるのに対し、尿細管周囲毛細血管は”第2の毛細血管”となっています。
また、下の腎臓の部分拡大図中央に尿細管周囲毛細血管が出ています。
重箱の隅をつつくような粗探しをしている理由は、クレアチニン値がほぼ半減した症例が2例あり(1人は3.64→1.82、もう1人は3.50→1.86)、「本当に不可逆的なのだろうか?」という疑問を払拭できないためです。
このお二人は、生活習慣の改善に努められている以外は、他の治療等はされていないため鍼治療が改善に貢献したのは間違いないと考えています。
今回、『血管内皮細胞をめぐる疾患』を拝読したのも、鍼治療の効果を裏づけるヒントが何か見つかるかもしれないという期待からです。
内容は極めて専門性が高く、消化できない内容でした。そこで、ブログは目次に続き、概要だけでも掴みたいため、“序”の大部分を書き出しました。そして、一番の関心事の“慢性腎疾患”については、理解のために、内容を吟味しながら箇条書きに整理していくということを行いました。
目次
序
基礎
1 血管内皮の構造
1.血管内皮細胞の一般的構造
2.様々な血管内皮細胞
2 血管新生と内皮前駆細胞
1.胎生期における血管新生
2.血管内皮前駆細胞の存在
3.血管内皮前駆細胞の動態
4.血管内皮前駆細胞の病態への関与とその治療応用
3 生理活性物質
ⅰ 血管収縮作動性物質
1.エンドセリン
2.アンジオテンシンⅡ
3.プロスタグランディンH₂(PGH₂)とトロンボキサンA₂(TXA₂)
ⅱ 内皮由来血管拡張物質
1.NO
2.内皮由来過分極因子 endothelium-derived hyperpolarizing factor(EDHF)
3.アドレノメデュリン
4.C型ナトリウム利尿ペプチド(CNP)
5.プロスタサイクリン
4 血管内皮細胞の傷害のメカニズム
1.NOとeNOS
2.血管内皮細胞におけるeNOS活性化の障害
3.酸化ストレスの亢進
5 血管内皮機能の測定法
1.血管内皮細胞の機能
2.ヒトにおける血管内皮機能評価法
3.内皮機能計測の今後
臨床
1 高血圧症
1.内皮機能障害と血管病変との関連
2.内皮機能障害とNO
3.内皮機能障害と酸化ストレスの関連
4.降圧薬と血管保護作用
2 高脂血症
1.粥状動脈硬化の病変
2.血管内皮細胞への単球・リンパ球の多段階の接着機構
3.粥状動脈硬化の病変部位に発現する接着分子
4.酸化LDLによる血管内皮細胞の機能障害
5.酸化LDLに対する受容体
6.血管内皮前駆細胞
3 糖尿病
1.プロテインキナーゼCの関与
2.Advanced glycation endproductsの関与
3.酸化ストレスの関与
4.インスリン抵抗性の関与
5.炎症の関与
4 肥満・メタボリック症候群
1.肥満・メタボリック症候群における血管内皮機能障害
2.メタボリック症候群における血管内皮機能障害発症機序
3.メタボリック症候群における血管内皮機能障害の治療
5 冠動脈疾患
1.冠動脈疾患のなりたち
2.冠動脈硬化巣の形成における血管内皮の役割
3.動脈硬化巣の進展
-動脈硬化性狭窄による狭心症の発症と動脈硬化巣の不安定化による急性冠症候群の発症-
4.血管内皮機能を改善することにより冠動脈疾患の発症を予防することはできるか?
6 慢性腎疾患
1.糸球体内皮細胞障害と腎障害機序
2.各種病態と糸球体内皮細胞障害
7 脳血管疾患
1.閉塞性脳血管障害と血管内皮細胞
2.出血性脳血管障害と血管内皮細胞
8 DIC
1.DICの血管内皮
2.DICとNO
3.eNOSの発現調節
4.eNOSからのスーパーオキシド産生
5.DICとCOガス
6.抗DIC薬と内皮細胞
9 膠原病
1.膠原病における止血凝固異常
2.全身性エリテマトーデス(SLE)における血管障害
3.抗リン脂質抗体症候群と血管障害
4.その他の膠原病と血管内皮障害
序
『血管内皮細胞の本格的な研究は、1970年以前に臍帯静脈の内面にトリプシン処理を施して血管内膜の1層の細胞を遊離し培養することに成功したことから始まる。これを開始したのは日本の研究者である。その後欧米の研究者によって細胞生化学的手法による内皮細胞の同定法が開発されて以降、血管内皮細胞の研究は飛躍的に前進した。内皮細胞の機能は、血液と血管壁を1層の細胞で隔てるのみに留まらないことがこの培養細胞を用いた研究によって次々に明らかになった。すなわち血小板凝集抑制作用や血管弛緩作用をもつプロスタサイクリンの生成、血管弛緩作用を有するNO[一酸化窒素]の遊離に関する発見は、後に両方ともノーベル賞が与えられた[前者は1982年ですが、物質はプロスタグランジン:PG(プロスタサイクリン:PGI2はプロスタグランジンの一つ)での受賞のようです。後者は1998年に受賞されています]。この事実によっても血管内皮細胞が生物科学の分野でいかに重要な位置を占めているかがわかる。その後、トロンボモジュリンが凝固系の抑制因子として、プラスミノーゲン活性因子(t-PA)およびその阻害因子(PAI-1)が線溶系の調節因子として、さらに日本人によってエンドセリンが内皮由来血管収縮因子として発見された。流血中の白血球を補足し結合させる因子として細胞表面付着分子(ELAM)が同定されて以降、様々な血管内皮細胞表面の細胞付着因子と白血球との相互反応の機序が解明された。まさに血管の生理的機能をマスターコントロールしている細胞、それが内皮細胞である。内皮細胞にはそれだけの機能を発揮できる分子機構が備わっている。同時に、毛細血管レベルまで含めると、血管内皮細胞の面積は肝臓などに匹敵する1つの臓器に例えられるくらい膨大なものになり、流血中の因子と血管表面の反応の広範な場を提供していることに今更ながら気づいたのである。
したがって内皮細胞がひとたび機能不全を起こすと、それは様々な疾患に結びつくことは容易に理解できる。最も端的な例は、冠動脈形成術の経験である。カテーテルで血管の内膜を障害してしまうと、血管はたちどころに血栓で覆われ動脈閉塞の危機にさらされることになる。内皮が修復されてはじめてその危機は去る。内膜表面は一見正常だが、もっと微妙な障害が内皮細胞に発生していることが様々な病態で明らかとなった。動脈硬化、それに関連する高脂血症、糖尿病、高血圧、心不全、喫煙、そして加齢が内皮機能不全を惹起する。ここで重要なことは、このような内皮機能不全は、このような病態が出現する前から検出されることである。すなわち動脈硬化性疾患発症のリスク因子はすなわち内皮機能不全のリスク因子でもあり、いかに血管の病態生理に内皮細胞が中心的役割を果たしているのかがわかる。内皮機能不全の原因もしくは促進因子として現在考えられている主要なものは「酸化ストレス」と「炎症反応」である。
内皮機能不全の病態生理の中心は、NO代謝の異常と考えられている。NO代謝に異常をきたすものとして、感染、放射線、化学療法などの他に動脈硬化そのものやその関連病態が知られている。現在はいまだ研究段階だが実際の臨床の場で内皮機能不全を評価する方法も種々考案されている。血流依存症の血管弛緩作用がNOによって維持されていることを利用した臨床検査が現在最も一般的である。測定する血管床は冠動脈、上腕動脈や細動脈レベルなど必ずしも病変局所に留まらない。前者は血管造影や超音波によって血管径の変化を測定する。後者は、プレティスモグラフィーなどで血流量の変化を測定する。血管内皮機能不全はびまん性に生じている全身的な現象であると考えられている。冠動脈疾患やハイリスク集団など様々な病態においてこのようにして測定された血管内皮機能が後の血管事故発生の予後と関連することが報告されている。血管内皮機能は、たいへん有益な情報をわれわれに与えてくれるはずであり、より一般的に測定評価できるシステムの開発が喫緊の課題である。
NO代謝を正常に保つ手段としては、運動、体重減少、食事療法などの生活習慣修正以外に種々の薬物療法も試みられている。L-アルギニン、N-アセチルシステイン、スタチン、ビタミンC、葉酸、アスピリン、エストロゲン、レニン-アンジオテンシン系阻害薬などがNO代謝を改善し内皮機能を正常化することにより心血管疾患の予後を改善することが報告されており、大いに期待されている。
本書は、現在わが国で最も活発にこの分野を研究している方々による「内皮細胞と疾患」をめぐる総説である。基礎研究者のみならず臨床家にとっても有益な内容になったと信じている。旧くて新しい内皮細胞の研究成果をアップデートすることの一助となれば幸いである。』
6 慢性腎疾患
●腎臓における血管内皮細胞としては糸球体内皮細胞が重要である。
●糸球体内皮細胞は糸球体の血管内腔を覆う1層の細胞で有窓構造をなし、糸球体基底膜の形成に関わっている。
●糸球体内皮細胞は血液中の種々のメディエーターや刺激により内皮細胞由来の様々な生理活性物質を放出し、メサンギウム細胞などの他の細胞と相互作用を生み出している。
●糸球体内皮細胞は相互作用を通じて、血管透過性、凝固線溶系、免疫機能、腎血行動態など多岐にわたる機能を有している。
1.糸球体内皮細胞障害と腎障害機序
●糸球体内皮細胞の障害には、白血球、炎症サイトカインや増殖因子、免疫複合体、血小板などに加えて腎血行動態などが複雑に関与している。
●NO(一酸化窒素)は内皮型NO合成酵素(eNOS:endothelial nitric oxide syntase)により産生される。
●NOは血管平滑筋拡張による腎内血行動態の調節作用や腎保護作用を有する。
●血管内皮細胞障害から糸球体障害に至るプロセス
“白血球活性化”(図右上)⇒【内皮細胞障害/活性化】
・細胞接着因子(ICM-1、P-セクレチンなど)が白血球を活性化する。
・炎症性サイトカイン(TNFα、IL-1βなど)が白血球を活性化する。[ILはインターロイキン]
・糸球体内では糸球体上皮細胞が血管内皮細胞増殖因子(VEGF)を産生して糸球体内皮細胞構造維持に関わっている。
・糸球体内ではメサンギウム細胞が肝細胞増殖因子(HGF)を産生して糸球体内皮細胞構造維持に関わっている。
【内皮細胞障害/活性化】⇒“eNOS”(図左中央)
・糸球体内皮細胞障害はeNOS(内皮型NO合成酵素)を低下させる。
・低下したeNOSは、凝固因子や血小板の活性化と相まって血栓形成や血管拡張機能不全の原因になる。
2.各種病態と糸球体内皮細胞障害
[1]糸球体腎炎
●内皮細胞障害により糸球体内では、基底膜陰性荷電の低下による蛋白尿が出現する。
●血栓形成増加や血管拡張障害による腎内血行不全が多くの腎疾患で惹起される。
●慢性腎疾患の進展には、活性酸素種、脂質、AGE(最終糖化蛋白)、サイトカインなどが複雑に関与している。
[2]腎不全
1)急性腎不全(ARF:acute renal failure)
●特に虚血性急性腎不全において血管内皮細胞障害が虚血性腎不全の病態進展に関わっている。
1.虚血性急性腎不全は、腎血流流量低下により初期には腎尿細管上皮細胞障害が生じる。
2.腎皮髄境界部や髄質外層部を中心に伴う低酸素状態および炎症反応持続的進行が起きる。
3.腎内微小循環の鬱滞や凝固系の活性化も伴う。
●虚血性障害は腎内血管内皮細胞の構造および機能障害を助長する。
●『最近では、虚血性ARF[急性腎不全]の治療戦略としてまだ実験段階ではあるが、内皮細胞障害を促進する凝固系因子および活性酸素種や接着因子を抑制する試みが始まっている。』
2)慢性腎不全(CRF:chronic renal failure)
●慢性腎不全は各種慢性腎疾患の進行により糸球体硬化病変増加により進展する。
●慢性腎不全は心血管疾患など、動脈硬化病変の合併リスク要因となる。
●慢性腎不全は病態の進展に血管病変が深く関わっている。
●慢性腎不全では慢性的な炎症反応が病変の進行や動脈硬化病変発症に関与する。
●『今後、CRF[慢性腎不全]の血管内皮機能障害を修飾する因子から治療への応用が期待される。』
[3]膠原病関連腎疾患
●『膠原病の合併症として腎病変は比較的多いが、本項ではいくつかの膠原病関連疾患における糸球体内皮機能障害を中心に述べる。』
1)ループス腎炎
●ループス腎炎は免疫複合体が糸球体内皮細胞下腔に沈着し、糸球体基底膜からの剥離をきたす。
●管内増殖性糸球体腎炎像を呈する時は、好中球、単球、リンパ球の内皮細胞への浸潤をきたし、糸球体内皮細胞は腫大や糸球体基底膜からの剥離を生じる。
●糸球体内皮機能障害の機序として、免疫複合体、坑内皮細胞抗体などがある。
2)強皮症腎
●腎臓の弓状動脈や小葉間動脈狭窄をきたし、腎皮質血流低下を生じる。このため、糸球体内も虚血となり糸球体内皮細胞の腫大や糸球体基底膜からの剥離がみられる。
●臨床的には急激に発症する悪性高血圧、腎不全を呈する強皮クリーゼが重要である。
3)ANCA関連腎炎
●ANCA関連腎炎は、病態に抗好中球細胞質抗体(anti-neutrophil cytoplasmic antibody:ANCA)が関与する腎病変である。
●ANCA関連腎炎における糸球体内皮細胞障害はANCAにより活性化された好中球が内皮細胞に接着し引き起こされる。さらに活性化された単球は炎症性サイトカインの産生を引き起こし、糸球体内皮細胞や血管内皮細胞障害を進展させる。
●ANCA関連腎炎の進展に血管内皮細胞障害が関連している。
●膜性増殖性糸球体腎炎や紫斑病性腎炎では糸球体内皮細胞下への免疫複合体の沈着による内皮細胞障害がみられる。
[4]糖尿病性腎症
●糖尿病性腎症では腎組織に細胞接着因子やケモカイン発現とマクロファージの浸潤がみられ、炎症性機序による糸球体内皮細胞障害が考えられる。
●糖尿病での内皮細胞での接着分子発現は高血糖による浸透圧上昇、酸化ストレス、AGE、糸球体内血行動態変化(糸球体過剰濾過など)によるshear stress[ずり応力]亢進などが複雑に関与している。
●Ⅱ型糖尿病の腎機能障害の進展に血管内皮細胞機能障害の関与が指摘されている。
[5]血栓性微小血管症(TMA:thrombotic microangiopathy)
●血栓性微小血管症は細動脈の内皮細胞障害により血小板血栓が形成され、赤血球の破砕と循環障害により臓器不全を生じる病態である。
[6]播種性血管内凝固症候群(DIC:disseminated intravascular coagulation syndrome)
●播種性血管内凝固症候群では、悪性腫瘍、各種感染症、産科疾患、熱傷などの基礎疾患を基盤として血小板、血液凝固線溶系、補体系などの活性化が生じる。このため、全身で微小血栓形成を引き起こし多臓器不全や出血傾向をきたす病態である。
●腎臓では糸球体内のフィブリン血栓が重要で、臨床的には急性腎不全を認めることが多い。
●糸球体内皮細胞障害としては、内腔の膨化、空胞化、基底膜剥離などがみられる。
●『最近は、DICの早期診断には凝固止血マーカーのみならず内皮細胞障害(トロンボモジュリンや接着分子)や白血球活性化(エラスターゼ、α1抗トリプシン)を示すマーカーの応用も期待されている。』
[7]妊娠中毒症(特に、子癇前症)
●妊娠中毒症は、妊娠中に高血圧、蛋白尿、浮腫のうち1つまたは2つ以上の症状がみられ、それらが妊娠偶発合併症でないものである。子癇前症は高血圧合併症が主体の病態で母体や胎児の障害、死亡率増悪に関わる病態である。
まとめ
1.血管内皮障害
●血管の内皮機能不全の原因もしくは促進因子として現在考えられている主要なものは酸化ストレスと炎症反応である。
●内皮機能不全の病態生理の中心は、NO代謝の異常と考えられている。
●糸球体硬化は内皮細胞の剥離が重要な因子となる。
2.慢性腎疾患(腎不全)
●慢性腎疾患の進展には、活性酸素種、脂質、AGE(最終糖化蛋白)、サイトカインなどが複雑に関与している。
“慢性腎疾患”の中で特に気になるのは“腎不全”ですが、注目したい点は5つです。
1)腎血流流量の低下
2)低酸素状態
3)血管病変
4)慢性的な炎症反応
5)血管内皮障害
★「何故、慢性腎臓病に鍼治療が効いたのか」については、いつか核心に迫れるように、地道な勉強を続けていきたいと思います。
ご参考
“こちらも『病気がみえる vol.8 腎臓・泌尿器』の図です。題名は「治療の概観」となっています。なお、ESKDとは“末期腎不全”、CVDとは“心血管疾患”のことです。
「慢性腎臓病(CKD)」の上に「リスクファクター」とあり、その1つに“生活管理”がありますが、その内容は以下になります。
“肥満の是正”、“禁煙”、“運動”の3つが対策ということですが、運動の効果と鍼治療の効果にについて、お伝えしたいことがあります。(ブログ「がんと自然治癒力9」より)

テロメアは染色体の端に存在し、細胞が分裂するたびに短くなります。そして、テロメアは細胞の老化の速度を決定します。
テロメアの研究でノーベル賞を受賞された、ブラックバーン先生はこの著書の中で”運動が細胞内部にもたらすメリット”というお話をされています。

左がそのページです。書かれている内容は下記の通りです。
『運動は細胞の内部にさまざまな良い変化をもたらす。運動は短期的なストレス反応を起こすが、それが引き金になって、大きな回復反応が起きるからだ。運動によって体の分子は損傷を受け、損傷した分子は炎症を引き起こす可能性がある。だが、運動を始めてまもなく、オートファジーという現象が起き、細胞はまるでパックマンのように、細胞内の損傷した分子を食べてしまう。これにより、炎症を防ぐことができる。同じ実験をさらに続け、損傷した分子の数がオートファジーで追いつかないほど多くなると、細胞は速やかに死滅する。これは「アポトーシス」と呼ばれ、炎症や残骸を残すことのないきれいな死に方だ。運動にはまた、エネルギーを生産するミトコンドリアの数や質を向上させる働きもある。このようにして運動は、酸化ストレスを減少させている。運動を終えて体が回復しようとしているとき、体内ではまだ細胞の残骸の掃除が続いている。それによって細胞は、運動をする前よりもっと健康に、もっと丈夫になる。』
私は鍼治療でも同様な効果が期待できるのではないかと考えています。それは次のような考えからです。
「筋肉痛は運動によって筋線維が傷つくことが原因とされています。一方、鍼の太さは0.16mm(1番鍼)、刺して多くは無痛でも、分子レベルで考えればたいへんな衝撃です。この運動による筋線維への微細な損傷と鍼による筋線維への微細な損傷は、プロセスも規模も異なりますが、それぞれのダメージに対する体の反応(筋線維修復の過程)は同様ではないかと思っています。つまり、鍼治療は運動と同じように、オートファジーやアポトーシスという重要な機能を呼び起こし、体内を掃除して、結果的に健康状態を良くしているのではないかと思います。」